Lo spazio intorno a noi è pieno di diversi corpi fisici, che consistono in diverse sostanze con diverse masse. Corsi scolastici di chimica e fisica, informando il concetto e il metodo per trovare una massa di materia, ascoltato e dimenticato in sicurezza tutto ciò che è andato a scuola. Ma nel frattempo la conoscenza teorica acquisita una volta potrebbe essere necessaria nel momento più inaspettato.
Calcolo della massa della sostanza usando la densità specifica della sostanza. Un esempio - c'è un barile per 200 litri. Hai bisogno di riempire la canna di qualsiasi liquido, dire, birra leggera. Come trovare un sacco di barili pieni? Usando la formula della densità della sostanza P \u003d m / v, dove P è la densità specifica della sostanza, M - Messa, V - volume occupato, per trovare un sacco di canna completa è molto semplice:- Volumi di volume - centimetri cubici, metri. Cioè, la canna per 200 litri ha un volume di 2 m³.
- La misura della densità specifica è con l'aiuto delle tabelle ed è un valore costante per ogni sostanza. La densità è misurata in kg / m³, g / cm³, t / m³. La densità della birra della luce e delle altre bevande alcoliche può essere visualizzata su sito web. È 1025,0 kg / m³.
- Dalla formula densità p \u003d m / v \u003d\u003e m \u003d p * v: m³ \u003d 1025,0 kg / m³ * 2 m³ \u003d 2050 kg.
Il volume del barile di 200 litri, completamente pieno di birra leggera, avrà un sacco di 2050 kg.
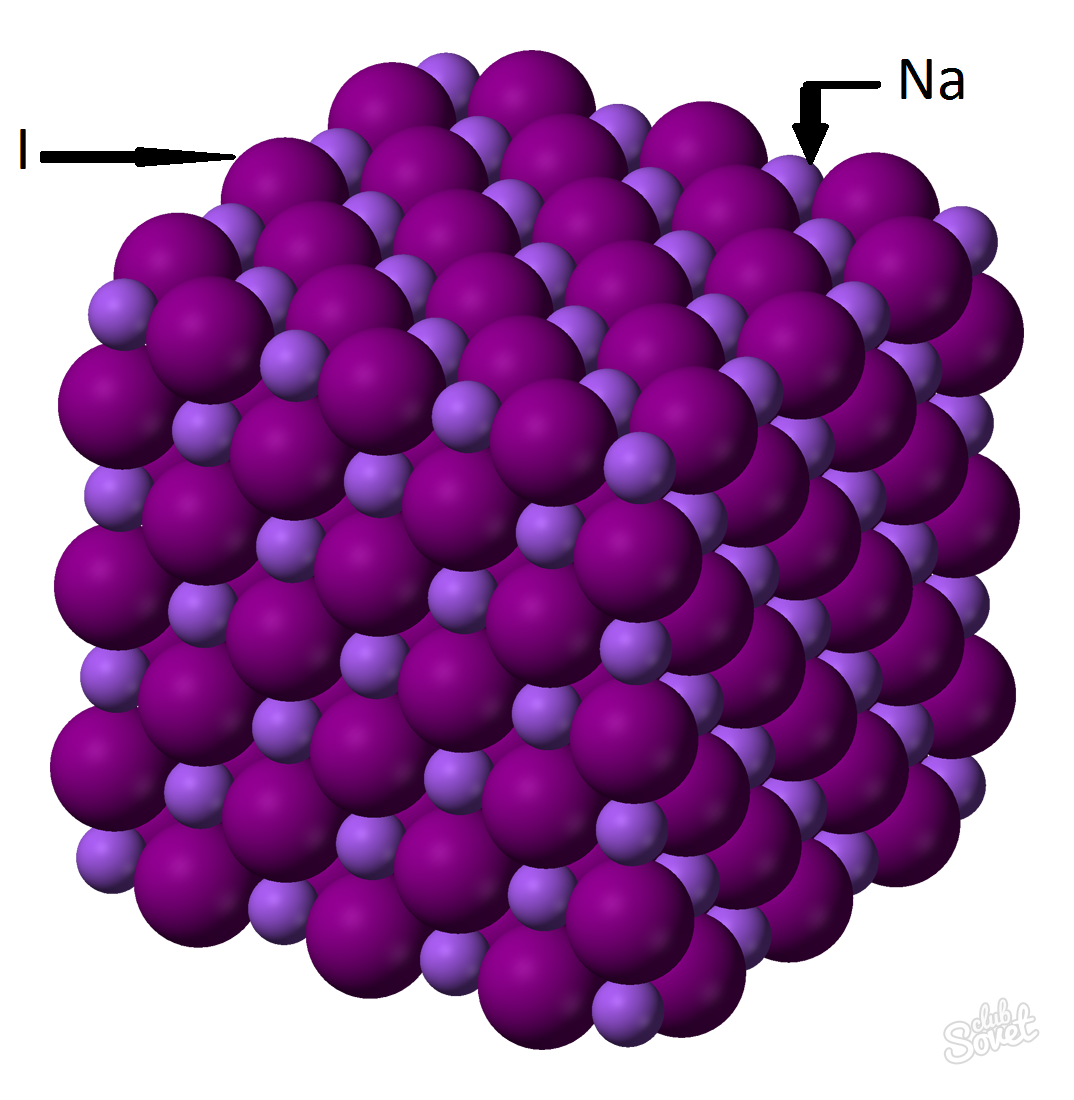
- La massa molare è calcolato in un unico sistema di misura S ed è misurata in kg / mol, g / mol. La massa molare di ioduro di sodio è la somma delle masse molari di ciascun elemento: M (NAI) \u003d m (nd) + m (i). Il valore della massa molare di ogni elemento può essere calcolato sul tavolo, ed è possibile con l'aiuto di un calcolatore online su sito web: M (NAI) \u003d M (Na) + m (i) \u003d 23 + 127 \u003d 150 (g / mol).
- Di formula generale M (NAI) \u003d M (NAI) / V (NAI) \u003d\u003e M (NAI) \u003d V (NAI) * M (NAI) \u003d 0,6 moli * 150 g / mol \u003d 90 grammi.
massa sodio ioduro (NAI) con una percentuale in massa di una sostanza di 0,6 moli è di 90 grammi.
- La diluizione con soluzione di acqua. La massa della sostanza disciolta X non cambia m (x) \u003d m '(x). La massa di soluzione aumenta sulla massa dell'acqua aggiunta M '(p) \u003d m (p) + m (H 2O).
- evaporazione dell'acqua dalla soluzione. La massa della sostanza disciolta X non cambia m (x) \u003d m '(x). La massa della soluzione diminuisce la massa della evaporazione dell'acqua M '(p) \u003d m (p) -m (H 2O).
- Digger due soluzioni. soluzioni di massa, così come la massa della sostanza disciolta X, la miscela è ripiegata: M '' (x) \u003d m (x) + m '(x). m '' (p) \u003d m (p) + m '(P).
- Perdita di cristalli. Le masse della sostanza disciolta X e la diminuzione soluzione sulla massa dei cristalli caduto: M '(x) \u003d m (x) -m (precipitato), M' (p) \u003d m (p) -m (precipitato) .

Opzioni che trovano una massa di una sostanza - un corso disconnesso di apprendimento scolastico e i metodi pienamente applicati nella pratica. Tutti possono facilmente trovare una massa della sostanza richiesta, applicando le formule sopra indicate e utilizzando le tabelle proposte. Per facilitare il compito, prescrivere tutte le reazioni, i loro coefficienti.