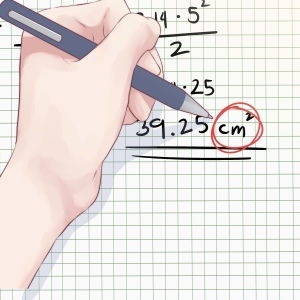L'espace autour de nous est rempli de différents corps physiques, qui consistent en différentes substances avec différentes masses. Cours d'école de chimie et de physique, informant le concept et la méthode de trouver une masse de matière, écouté et oublié en toute sécurité tout ce qui est allé à l'école. Mais pendant ce temps, les connaissances théoriques acquises par une fois peuvent être nécessaires au moment le plus inattendu.
Calcul de la masse de la substance en utilisant la densité spécifique de la substance. Un exemple - il y a un baril pour 200 litres. Vous devez remplir le baril de tout liquide, par exemple, la bière légère. Comment trouver beaucoup de barils remplis? Utilisation de la formule de densité de la substance P \u003d m / V, où p est la densité spécifique de la substance, m - masse, volume occupé par V, pour trouver beaucoup de baril complet est très simple:- Volumes de volume de volume cubique, mètres. C'est-à-dire que le baril de 200 litres a un volume de 2 m³.
- La mesure de la densité spécifique est à l'aide de tables et est une valeur constante pour chaque substance. La densité est mesurée en kg / m³, g / cm³, t / m³. La densité de la bière de la lumière et d'autres boissons alcoolisées peut être vue sur site Internet. Il est 1025,0 kg / m³.
- De la formule de densité p \u003d m / v \u003d\u003e m \u003d p * v: m³ \u003d 1025,0 kg / m³ * 2 m³ \u003d 2050 kg.
Volume de baril de 200 litres, entièrement rempli de bière légère, aura beaucoup de 2050 kg.
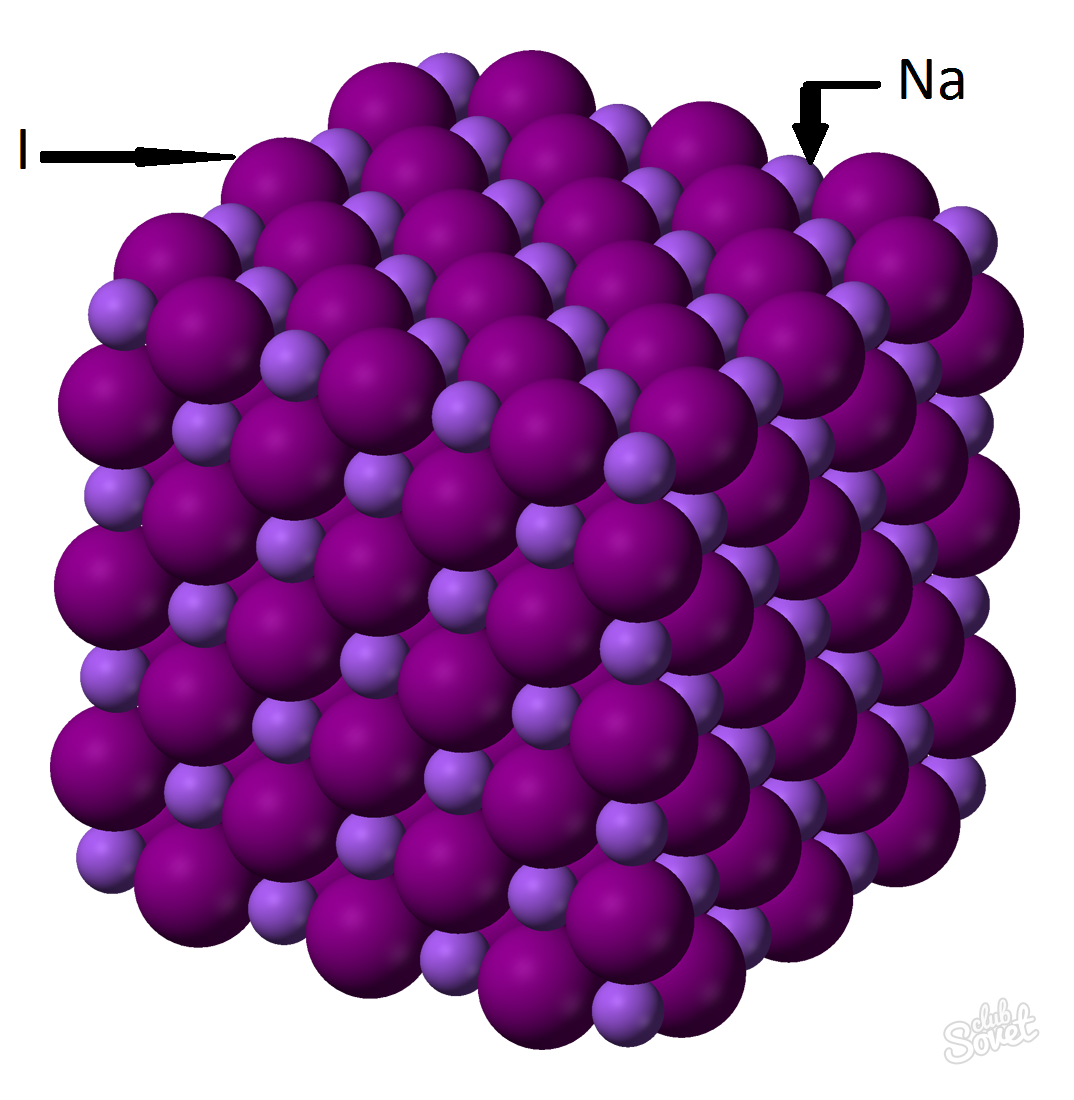
- Masse molaire est calculé de mesures individuelles SI et se mesure en kg / mol g / mol. Masse molaire d'iodure de sodium - est la somme de la masse molaire de chaque élément: M (NaI) \u003d M (Na) + M (I). masse moléculaire de chaque élément peut être calculé à partir de la table et peut utiliser la calculatrice en ligne sur site Internet: M (NaI) \u003d M (Na) + M (I) \u003d 23 + 127 \u003d 150 (g / mol).
- De la formule générale M (NaI) \u003d m (NaI) / v (NaI) \u003d\u003e m (NaI) \u003d v (NaI) * M (NaI) \u003d 0,6 mol * 150 g / mole \u003d 90 g.
Poids d'iodure de sodium (NaI) avec une fraction massique de substance de 0,6 mole de 90 grammes.
- La solution d'eau de dilution. La masse de la substance X dissous reste inchangée m (X) \u003d m « (X). solution de masse est augmentée par la masse d'eau ajoutée m « (p) \u003d m (p) + m (H 2O).
- L'évaporation de l'eau de la solution. Le poids du soluté ne change pas X m (X) \u003d m « (X). masse de la solution est réduite à la masse d'eau évaporée m « (p) \u003d m (p) -m (H 2O).
- La fusion des deux solutions. solutions sur les poids, ainsi que la masse de soluté X se replient en mélangeant: m '' (X) \u003d m (X) + m « (X). m '' (p) \u003d m (p) + m « (p).
- Laissez tomber les cristaux. Poids X soluté et de la solution sont réduits par rapport au poids des cristaux séparés: m '(X) \u003d m (X) -m (boues), m' (p) \u003d m (p) -m (boues).

Options Trouver une masse d'une substance - un cours déconnecté de l'apprentissage scolaire et les méthodes entièrement appliquées dans la pratique. Tout le monde peut facilement trouver une masse de la substance requise, en appliquant les formules ci-dessus et en utilisant les tables proposées. Pour faciliter la tâche, prescrire toutes les réactions, leurs coefficients.