Biz atrofida kosmik turli massasidan turli moddalar iborat turli jismoniy organlari bilan to'ldiriladi. kimyo va fizika, tushuncha va materiya massasini topish usuli xabardor maktabi kurslar, quloq va xavfsiz maktabga borib hamma narsani unutib. Lekin orada bir marta tomonidan sotib nazariy bilim eng kutilmagan paytda zarur bo'lishi mumkin.
moddaning solishtirma zichligi yordamida moddaning massasini hisoblash. Bir misol, - 200 litr uchun barrel bor. Siz har qanday suyuqlik, aytaylik, engil pivo barrel to'ldirish kerak. Qanday to'ldirilgan bochkalarni ko'p topish uchun? massasi, V - - P moddalar, M muayyan zichligi modda R \u003d M / V, zichligi formulalar yordamida bosib olingan hajmi, to'liq barrel ko'p juda oddiy topish uchun:- kub santimetr, metr, - hajmining hajmi. deb, 200 litr uchun barrel 2 m³ hajmi ega.
- solishtirma zichligini chora jadvallar yordamida hisoblanadi va har bir modda uchun doimiy qiymat hisoblanadi. zichligi, g / cm³, t / m³ kg / m³ o'lchanadi. engil va boshqa spirtli ichimliklarni pivo zichligi ustida ko'rish mumkin veb-sayt. Bu 1025,0 kg / m³ hisoblanadi.
- zichligi formula P \u003d m / V \u003d\u003e m \u003d p * v: m³ \u003d 1025,0 kg / m³ * 2 m³ \u003d 2050 kg.
to'liq engil pivo bilan to'ldirilgan 200 litr, bir barrel hajmi 2050 kg ko'p bo'ladi.
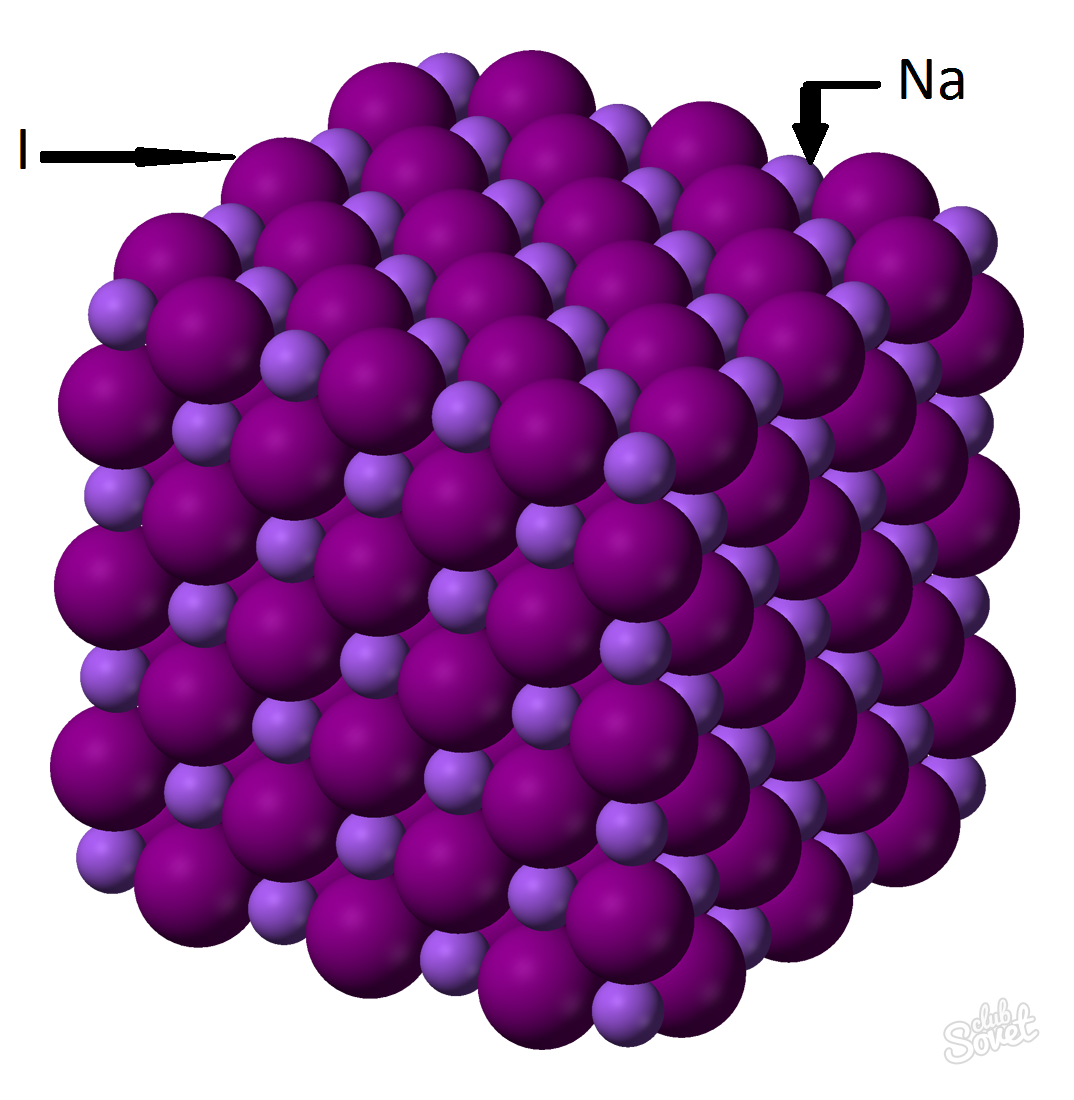
- Monlar massasi bitta o'lchash tizimida hisoblanadi va kg / Mol, g / mol ichida o'lchanadi. Natriy yodidning molyar massasi har bir elementning molyar massasi: m (nay) \u003d m (Na) + m (i). Har bir elementning molyar massasining qiymati stolda hisoblab chiqilishi mumkin va siz onlayn kalkulyator yordamida foydalanishingiz mumkin veb-sayt: M (nay) \u003d m (i) + m (i) \u003d 23 + 127 \u003d 150 (g / Mol).
- Umumiy formula m (nay) \u003d m (nay) / v (nay) \u003d m (nay) * m (nay) * m mol \u003d 90 gramm.
Natriy yodid massasi (NAI) 0,6 molning massa ulushi 0,6 molning massa ulushi 90 gramm.
- Suv eritmasi bilan suyultirish. Erigan x modda massasi m (x) \u003d m '(x) ni o'zgartirmaydi. Qo'shilgan suv massasining massasi ko'payadi m '(p) \u003d m (p) + m (h) 2O).
- Eritmadan suvning bug'lanishi. Esilangan moddaning massasi x (x) \u003d m '(x) ni o'zgartirmaydi. Eritma massasi suv m '(p) \u003d m (p) -m (h) massasiga kamayadi 2O).
- Ikki echimni qazuvchi. Mass echimlari, shuningdek, x eritilgan moddaning massasi, aralashmasi katlanmılırığı: m '' (x) + m '(x) + m' (x). m '' (p) \u003d m (p) + m '(p).
- Kristallarning yo'qolishi. Erigan modda x va echimning massasi pasayib ketdi: m '(x) \u003d m' (p) \u003d m (p) -m (p) .

Moddani topish variantlari - maktabni o'qitishning uzilgan kurslari va amalda to'liq qo'llaniladigan usullar. Har bir inson oson bo'lgan moddaning massasini topishi, yuqoridagi formulalarni qo'llash va taklif qilingan jadvallardan foydalanishni osongina topishi mumkin. Vazifalarni engillashtirish uchun barcha reaktsiyalarni, ularning koeffitsientlarini buyuring.