Prostor oko nas je ispunjen različitim fizičkim tijelima, koji se sastoje od različitih tvari s različitim masama. Školski tečajevi kemije i fizike, informiranje koncepta i metode pronalaženja mase materije, slušali i sigurno zaboravili sve što je išlo u školu. No, u međuvremenu, teoretsko znanje koje je jednom može biti potrebno u najneočekivanijem trenutku.
Izračunavanje mase tvari pomoću specifične gustoće tvari. Primjer - postoji bačva za 200 litara. Morate ispuniti cijev bilo koje tekućine, recimo, lagano pivo. Kako pronaći mnogo ispunjenih bačva? Koristeći formulu gustoće tvari p \u003d m / v, gdje je p specifična gustoća tvari, m - masa, v - okupirana volumena, za pronalaženje puno pune cijevi je vrlo jednostavno:- Volume volumena - kubičnih centimetara, metara. To jest, bačva za 200 litara ima volumen od 2 m³.
- Mjera određene gustoće je uz pomoć tablica i konstantna je vrijednost za svaku tvar. Gustoća se mjeri u kg / m³, g / cm³, t / m³. Gustoća piva svjetla i drugih alkoholnih pića može se promatrati web stranica, To je 1025,0 kg / m³.
- Iz formule gustoće p \u003d m / v \u003d\u003e m \u003d p * v: m³ \u003d 1025,0 kg / m³ * 2 m³ \u003d 2050 kg.
Barrel Volumen od 200 litara, potpuno ispunjen laganim pivom, imat će mnogo 2050 kg.
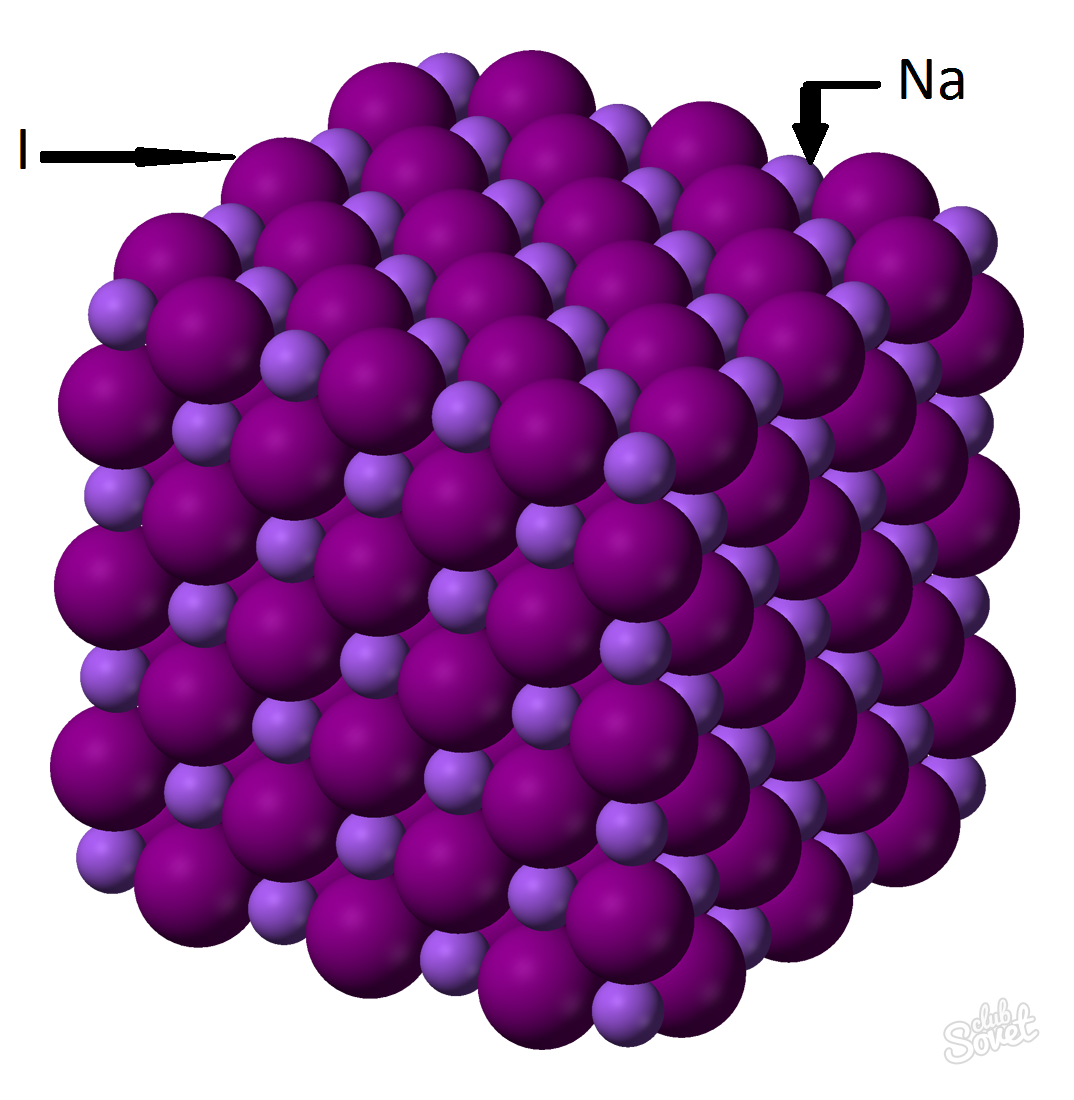
- Molarna masa se izračunava u jednom mjernom sustavu s i mjeri se u kg / mol, g / mol. Molarna masa natrijevog jodida je zbroj molarnih masa svakog elementa: m (NaI) \u003d m (Na) + m (i). Vrijednost molarne mase svakog elementa može se izračunati na tablici, a možete uz pomoć online kalkulatora web stranica: M (NaI) \u003d m (Na) + m (i) \u003d 23 + 127 \u003d 150 (g / mol).
- Opće formule M (NAI) \u003d m (NAI) / v (NaI) \u003d\u003e M (NaI) \u003d v (nai) * m (NAI) \u003d 0,6 mol * 150 g / mol \u003d 90 grama.
Natrijeva jodidna masa (NAI) s masenim frakcijama tvari od 0,6 mola je 90 grama.
- Razrjeđivanje s vodom otopinom. Masa otopljene X tvari ne mijenja m (X) \u003d m '(X). Masa otopine se povećava na masi dodane vode M '(p) \u003d m (p) + m (h 2O).
- Isparavanje vode iz otopine. Masa otopljene tvari X ne mijenja m (x) \u003d m '(X). Masa otopine se smanjuje na masu isparavanja vode M '(p) \u003d m (p) -m (h 2O).
- Dva rješenja. Masovna otopina, kao i masa otopljene tvari X, smjesa je presavijena: M '' (X) \u003d m (X) + M '(X). m '' (p) \u003d m (p) + m '(p).
- Gubitak kristala. Mase otopljene tvari X i otopina se smanjuju na masi kristala palože: M '(X) \u003d m (X) -m (talog), M' (p) \u003d m (p) -m (precipitat) (talog) ,

Opcije Pronalaženje mase tvari - nepovezani tijek učenja škole i metode u potpunosti primijenjene u praksi. Svatko može lako pronaći masu potrebne tvari, primjenjujući gore navedene formule i koristeći predložene tablice. Da biste olakšali zadatak, propisuju sve reakcije, njihove koeficijente.